碳化法制拟薄水铝石反应机理
碳化法是指偏铝酸钠溶液中通入 CO2进行沉淀制备拟薄水铝石的方法,实际是碱法中的一种。由于该法也是工业上生产氢氧化铝的主要方法,所以单独称之为碳化法,或者碳酸法。
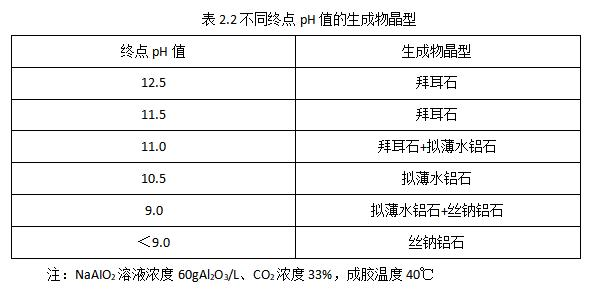
以偏铝酸钠为底液,不断通入CO2,随着中和终点 pH 值不同,产物结构各不相同,表 2.2 给出了终点 pH 值对生成物类型的影响。当终点 pH 值从 12.5 变化至 10.5 时,生成物从β1-AI(OH)3变成拟薄水铝石;继续降低 pH 值至 9.0,出现拟薄水铝石与丝钠铝石(dawsonite);终点 pH 值继续降低,则产物全部为丝钠铝石。碳化法产物和终点 pH 值的关系与其他方法类似又略有不同,比如 NaAIO2-HNO3法、AICI3-NaOH 法、NaAIO2-Al2(SO4)3法等在 pH 值不断变化的成胶过程中,如果加料方法属于反加法,即体系 pH 值逐渐降低,通常是无法制备出拟薄水铝石的,但偏铝酸钠溶液中加入 CO2却能制备拟薄水铝石。
通常 NaAIO2溶液的苛性系数 αk=1.4~1.8,CO2加入 NaAIO2溶液的成胶过程存在四种反应:NaOH 与 CO2快速中和反应、NaAIO2与 CO2中和反应、NaAIO2水解反应,以及 CO2与生成的水合氧化铝及 Na2CO3的复合反应,化学反应方程式如下:
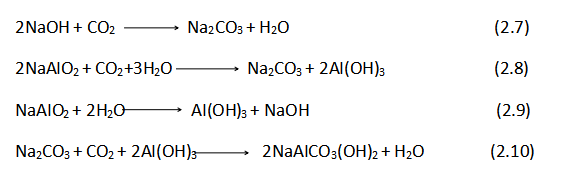
反应式(2.8)生成的水合氧化铝在合适条件(合适的 pH 值和温度等)下经老化转化为拟薄水铝石,反应式(2.9)生成的水合氧化铝为 β-Al2O3·3H2O 或 α-Al2O3·3H2O,反应式(2.8)与反应式(2.9)是平行反应。因此,碳化法成胶过程中生成的水合氧化铝究竟是拟薄水铝石(老化后)、拟薄水铝石与 β1-AI(OH)3的混合物,还是β1-AI(OH)3,主要取决于式(2.8)与式(2.9)的反应速度及反应程度。反应速度主要取决于成胶温度、CO2流量及浓度,而反应程度主要取决于反应终点 pH值。
温度较高(>80℃)时,式(2.9)反应速度较快,NaAlO2溶液中通入CO2气体,首先进行式(2.7)的反应,溶液的苛性系数急剧降低,其稳定性被破坏,溶液发生式(2.9)的反应,生成氢氧化铝和 NaOH,水解生成的 NaOH 继续与CO2反应,使得式(2.9)持续进行。氧化铝工业上的“碳分法”制取氢氧化铝就是基于这个原理。为阻止生成的氢氧化铝中引入过量的硅,反应终点一般控制在终点 pH 值为 11.0 以上,中和反应生成的无定形水合氧化铝和小晶粒拟薄水铝石经老化后几乎全部转化为大晶粒的氢氧化铝,有利于后续电解生产金属铝。
在较低成胶温度及较大的 CO2流量与浓度下,NaAIO2溶液的中和反应式(2.8)占主导地位,在终点 pH 值为 10.5 时,生成的无定形水合氧化铝和小晶粒的拟薄水铝石,经老化后转化为无杂晶的大晶粒拟薄水铝石。
低温成胶且终点 pH 值较高(≥11.0)时,NaAIO2溶液由于被 CO2中和,其苛性系数降低(ak接近 1)。虽然中和反应已结束,但未被中和的 NaAlO2极不稳定而发生水解,生成β1-AI(OH)3和 NaOH,且在高 pH 值的老化过程中,中和生成的无定形水合氧化铝及小晶粒拟薄水铝石部分或全部转化为 β1-AI(OH)3且终点 pH 值越高,越易于转化完全。由于β1-AI(OH)3比拟薄水铝石有更高的稳定性,一旦成胺过程生成 β1-AI(OH)3通常条件下很难再转化为拟薄水铝石。低温成胶且终点 pH 值(<9.0)较低时,生成的水合氧化铝和 CO2及 Na2CO3继续反应,发生式(2.10)的反应,生成丝钠铝石,化学式为 NaAICO3(OH)2。
因此,碳化法制备拟薄水铝石时,通入的 CO2既要有足够的流量,又要有足够的反应,这是碳化法虽然加料方式为反加法却能制备拟薄水铝石的有力保证。


